本文是專業學術論文解讀,不做醫療建議。
過去,想了解移植器官的狀態,往往要“反覆穿刺”做一系列活檢。如今,研究人員巧妙設計了一種留在體內工作的微型傳感器,並在完成使命後自行安全降解。
近期,美國達特茅斯學院歐陽偉教授團隊開發了一款可編程、可生物吸收的微針傳感器陣列,可用於監測器官功能衰竭和移植器官狀態等。
在器官移植手術中,醫生將該設備放置在患者體內,它可以像電子紋身那樣緊密貼合在組織表面。不侷限於二維平面,它還能作爲原位探針刺破器官表面黏膜,通過微創方式對器官內部微環境直接進行實時、穩定、多通道的健康監測,未來有望避免重複性的有創活檢、放射性的計算機斷層掃描(CT)或磁共振成像(MRI)檢查等。
結果顯示,該設備在腎缺血和腸道疾病等病症的動物模型中,實現了連續 7 天以上監測多種關鍵生化和生理指標,如葡萄糖、乳酸、氧氣分壓、電解質等,它們對於術後第一週瞭解患者的器官狀態尤爲重要。
有意思的是,完成監測任務後,研究人員可啓用設計程序將該設備逐步安全降解。也就是說,該設備在完成任務後可安全“消失”,降低了患者二次手術帶來的風險和負擔。
“它不僅是器官表面的貼附式傳感器,更是可消失的、微創介入式器官生化以及生理功能的監測平臺。該技術在圍手術期和重症監護監測方面具有潛力,尤其是對於捕捉缺血、代謝紊亂或炎症等早期變化尤爲關鍵。”該論文第一作者、達特茅斯學院博士後研究員李湘凌對 DeepTech 表示。(注:圍手術期是圍繞手術的全過程,包括術前、術中和術後階段。)

圖丨左起:李湘凌、歐陽偉(來源:李湘凌、達特茅斯學院官網)
審稿人對該研究評價稱:“該研究填補了圍手術期護理中的關鍵空白,工程創新與轉化設計標誌着向臨牀可行、可植入的器官健康診斷技術邁出了重要一步。”
相關論文以《一種用於圍手術期器官健康監測的可編程、生物可吸收的電化學微針傳感器陣列》(A programmable bioresorbable electrochemical microneedle sensor array for perioperative monitoring of organ health)爲題發表在 Nature Biomedical Engineering 上[1]。達特茅斯學院博士後研究員李湘凌是第一作者,歐陽偉教授擔任通訊作者。

圖丨相關論文(來源:Nature Biomedical Engineering)
受蜜蜂尾針啓發,讓微針易於刺入組織,難以脫落
現階段,臨牀醫生主要通過監測心率、血壓和血氧等生命體徵,來判斷患者器官的相關症狀。如果病情嚴重,還會通過 B 超、CT 和 MRI 等設備進一步檢查,以及使用活檢來對器官進行最終判斷。
長期以來,深部器官在圍手術期始終缺乏能夠連續、具有原位功能的監測手段,這也導致了併發症的“後知後覺”——往往在患者出現顯著症狀後才被發現,例如,缺血、代謝紊亂或功能恢復不良等。特別是對於腎移植或肝移植患者來說,及時瞭解器官的狀態有利於患病初期的干預。
然而,要實現這一點並非易事。深部器官表面溼潤、蠕動/搏動明顯(腸蠕動、腎臟隨呼吸位移),傳統貼附或直針結構容易滑移、脫落或造成剪切刺激。爲解決上述問題,研究人員研發了生物可吸收微針傳感器陣列,不僅能定製微針的直徑、長度和銳度,還設計了一種向後倒刺的獨特結構。
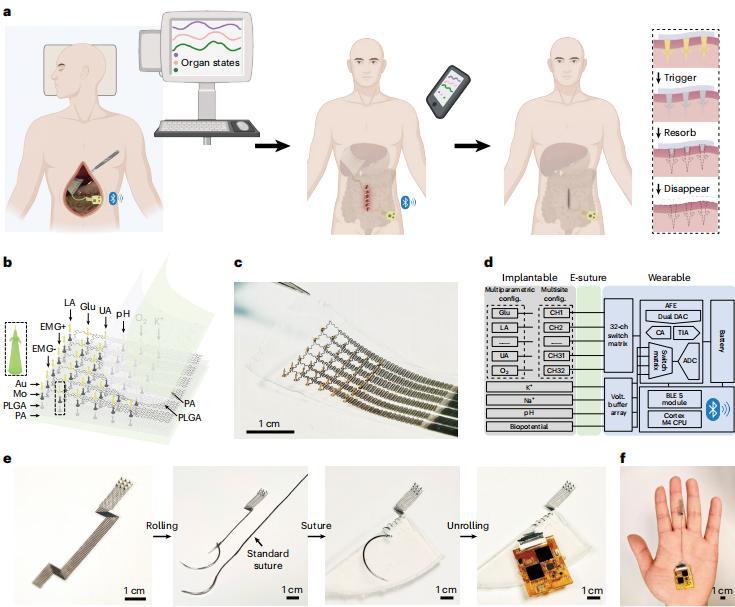
圖丨設計概念與系統特性(來源:Nature Biomedical Engineering)
據介紹,該結構的設計靈感來自蜜蜂尾針,其巧妙之處在於力學的不對稱性設計:微針易於刺入組織,但卻很難脫落。就像蜜蜂蜇人或動物後,尾針可能會留在後者組織上。結果顯示,這種結構在三排倒刺微針中的錨定力可提升至 71 倍。
如何在柔軟的襯底上加工倒刺結構的可降解微針,不僅是全新的探索更是巨大的挑戰。當時,研究人員嘗試了很多種方法,包括 4D 打印、磁流變光刻技術以及雙光子光聚合等。
然而,這些方法具有不同的侷限性:要麼只能加工硬性結構,無法在柔性襯底上操作;要麼無法在有限面積內實現高密度的微針陣列,因此都難以實現規模化應用。

圖丨基於 3D 打印且無需光刻技術的製造工藝的顯微照片與顯微圖像(來源:Nature Biomedical Engineering)
基於此,研究團隊提出了一種變形耦合的 3D 打印新策略,實現了在柔性襯底上加工高密度的微針倒刺陣列:首先打印出水平倒鉤的微針結構,再通過按壓的方法讓刺向下彎曲形成穩定的倒刺。
李湘凌指出,這種方法可實現大面積加工,目前展示了 6×6,理論上可以做 3D 打印平臺大小的尺寸。它不僅可以加工出大量倒刺,而且微針和倒刺的間距都能做得很密集。
讓設備自動消失的“魔法”
除了加工方面的挑戰,研究團隊還面臨電子模塊的集成問題。爲此,他們結合最新的嵌入式電路技術,實現了電子模塊的多路複用。在本次研究中針對小動物實驗使用了 3×3 陣列(9 個針頭),針對大動物可以使用 6×6 陣列(36 個針頭)並加工出 32 個通道的開關矩陣,支持對 32 個位點同時進行多模式監測。
在生物安全性方面,該團隊借鑑連續性血糖儀針頭的塗層技術,使用了具有抗污性能的聚氨酯(PU)和聚乙二醇(PEG)複合塗層。通過結合二者的優勢,研究人員在活體大鼠腎臟中,實現了微針陣列可穩定植入 7 天以上。多次實驗結果顯示,其信號強度通常在 80% 以上,爲長期和穩定的信號採集奠定了基礎。
目前臨牀上的金標準是活檢,但它需要穿刺器官部位取樣,頻繁活檢給患者帶來身心創傷。“相比之下,我們的設備是一種微創、負擔小的解決方案。使用後可以在體內自然降解,不會對患者造成二次傷害。”李湘凌表示。

(來源:Nature Biomedical Engineering)
那麼,這種微針陣列是如何在監測任務結束後自我降解的呢?
微針主體材料採用聚乳酸-羥基乙酸共聚物(PLGA)製成,這種材料可通過水解促進生物吸收。爲實現同時監測多種關鍵指標,微針陣列由不同功能的傳感器組成,並在其外部塗覆多種電極材料,例如金(Au)、鉑(Pt)、銀/氯化銀(Ag/AgCl)等。
人體內環境比較複雜,存在各種導電離子。當金與氯離子(如生理鹽水中的氯化鈉)接觸且在通電驅動條件下,會加速變成可溶解的氯金酸根離子。研究團隊利用電解原理,當設備通電時通過可編程、可程序控制的設計,提供 1.95 伏以上的電壓驅動,使傳感針頭上的金溶解。
歐陽偉教授解釋道:“在微針陣列設備中金是最難降解的物質,其他材料都是已通過醫用或美國食品藥品監督管理局(FDA)認證的可降解材料。這些材料或金屬均能在體內穩定存在。當金溶解後,其他部分可逐步被生物吸收並經體內途徑清除。”
推動術後監護從間歇檢查走向連續感知
李湘凌此前在中山大學獲得博士學位,目前正在達特茅斯學院歐陽偉教授課題組從事博士後研究。研究的重點是開發生物工程醫療設備,尤其是面向老齡化社會需求的微創、連續監測與智能干預型醫療器件。
人口老齡化是全球面臨的共同問題,隨之而來的是健康監測管理需求顯著上升。例如,重大慢性疾病包括糖尿病、高血脂、高血壓等代謝性及代謝相關疾病,以及癌症、器官移植圍手術期併發症及其術後長期管理等。從某種程度上來說,精準連續監測和智能化干預醫療器件的水平與老年人晚年生活的質量密切相關。
如果能夠通過開發先進的設備和技術,對患者病情進行及時、連續的監測與干預,不僅有助於在疾病發生的早期實現精準識別,還可有效阻止疾病的進一步惡化。
李湘凌舉例說道:“以糖尿病等慢性疾病爲例,嚴格而持續的血糖監測是實現疾病長期控制的關鍵。此外,能夠準確地監測早期的生物標誌物,例如腫瘤細胞相關的核酸,就有可能會防止其形成惡性腫瘤甚至拯救生命。這些都具有很重要的意義,也是我從事該領域研究的主要動力來源。”
本次研究所開發的微針傳感器陣列在不增加患者額外負擔的前提下,實現了對深部器官多種生化指標的連續監測,且使用後能直接安全地消失,爲術中決策和術後早期干預提供了一種更直接、更及時的依據。
該技術可用於監測器官功能衰竭和監測移植器官。在這項研究中,研究人員已經驗證了它在腸道代謝紊亂和腎臟缺血情況下的應用,但由於目前動物模型的限制,實驗條件還不足以模擬更接近臨牀的真實環境。
在接下來的研究階段中,研究人員希望在器官移植方面得到臨牀方面支持,通過將設備植入體內,監測器官移植過程中生物標誌物的變化,並跟蹤器官移植後的狀態。
需要了解的是,由於人的身體尺寸與動物模型不同,如果將該設備應用於人體需要進一步調整。此外,人體對生物安全和信號穩定性方面的要求更高,需要尋找足夠生物相容的材料並提升信號穩定性,來滿足臨牀的實際需求。
此外,該平臺還有望擴展至炎症因子、疾病指標或藥物監測等。目前,歐陽偉教授研究團隊正在該方向探索並已獲得初步進展。
相比於在體監測代謝物、離子和組織氧含量的技術更有意義的方向,是監測與人體疾病相關的指標。因爲除了代謝物,更重要的指標還有細胞因子和相關蛋白質,能夠更加準確地反應移植器官的生理狀態。此外,在藥物監測方面,例如器官移植後需要使用的抗生素,以及用於判斷是否發生感染的標誌物等。
更長遠地來看,未來這類設備廣泛應用於臨牀,有望徹底改變患者手術後的監護模式。從間歇檢測到持續感知,這類“可消失”的監測設備,讓我們看到了術後監護方式的更多可能性。
參考資料:
1.https://doi.org/10.1038/s41551-025-01609-z
運營/排版:何晨龍
本文是專業學術論文解讀,不做醫療建議。





