本文是專業學術論文解讀,不做醫療建議。
作爲一類新型免疫療法,嵌合抗原受體 T 細胞(CAR-T)療法近年來在癌症治療領域取得了巨大成功。它能在某些復發或難治性血液腫瘤中展現出驚人療效,爲使用其他治療均失敗的患者帶來持久緩解的希望。
然而,其高度個性化的體外製備流程不僅耗時耗力、成本高昂,還要求患者在前期清除原有免疫細胞,這既增加了感染風險,也限制了該療法的普及。爲克服這些瓶頸,生物醫學領域的學者們一直在探索如何製造出成本更低、更安全、更具可及性的 CAR-T 產品,主流方案包括但不限於無需體外製造的體內直接工程 CAR-T、健康供體來源的異體現成 CAR-T,以及各類提高製造效率的工藝創新等。
近日,《自然》(Nature)雜誌同期刊發了一篇重磅研究論文及兩篇點評文章,重點介紹了體內直接工程 CAR-T 的突破性進展:科學家們成功利用 CRISPR 技術,在小鼠體內實現癌症免疫細胞的精準工程化。這或許預示着,未來只需一次簡單的注射,你體內的免疫細胞就能被精準改造,化身一支訓練有素的“抗癌特種兵”,直搗病竈,清除腫瘤。
(來源:Nature News)
CAR-T 療法的演進:從體外輸注到體內原位編程
CAR-T 細胞療法的原理是通過基因工程改造患者自身的 T 細胞,使其表面表達一種名爲 CAR 的人工合成受體,其能識別癌細胞表面的特異性抗原,從而激活 T 細胞,精準地識別、殺傷癌細胞。對於某些復發或難治性血癌,如白血病、淋巴瘤和骨髓瘤,CAR-T 細胞療法的效果遠超現有其他療法。
但現行的 CAR-T 療法制造過程複雜且成本高昂,極大地限制了其可及性。具體而言,醫生需要從患者體內抽血,分離出 T 細胞,然後在實驗室中利用病毒載體將 CAR 基因導入 T 細胞基因組,使其表達 CAR。接着,這些經過改造的 CAR-T 細胞需要在體外擴增、進行嚴格的質量檢測,最後再回輸到患者體內。
在此之前,患者還需要接受毒性較大的化療預處理,清除自身未經改造的免疫細胞,爲 CAR-T 細胞在體內擴增和發揮作用創造空間。這不僅增加了患者的痛苦,也使其在治療期間面臨更高的感染風險。
(來源:BBC/War in the Blood)
爲克服這些限制 CAR-T 療法推廣的因素,科學家們一直在積極探索“體內工程化”T 細胞的方法,直接在患者體內改造 T 細胞,使其獲得抗癌能力。這種方法一旦成功,不僅可以大大降低治療成本,簡化治療流程,甚至有望避免對身體傷害過大的預處理環節。
“起初,這聽起來像個瘋狂的想法,簡直是科幻小說。”該研究的通訊作者、加州大學舊金山分校的免疫學家賈斯汀·艾奎姆(Justin Eyquem)回憶道。早在 2017 年,他和同事們就曾利用 CRISPR-Cas9 技術,將 CAR 基因精準插入離體 T 細胞基因組的特定區域,顯著提高了 CAR-T 細胞的有效性。當時他們便開始思考,能否有一天在體內實現這一壯舉。
近年來,隨着基因編輯技術的不斷成熟,體內 CAR-T 細胞治療的研發取得了重要進展,首批相關療法已進入早期臨牀試驗。然而,安全性一直是體內基因編輯面臨的核心問題。例如,如果 CAR 基因被隨機插入 T 細胞基因組,可能會引發致癌突變;更重要的是,爲了保證治療安全,必須確保基因編輯只作用於 T 細胞,不誤傷其他細胞類型,尤其是生殖細胞。
CRISPR 技術構建共遞送系統,力求“直達靶心”
在這些安全性挑戰之下,研究團隊選擇利用 CRISPR 技術構建一套創新的體內基因編輯系統,實現 T 細胞的精準重編程。
他們的核心策略是採用兩向量遞送系統,其一是包膜遞送載體(EDV),即攜帶 CRISPR-Cas9 基因編輯所需的 Cas9 蛋白和引導 RNA(gRNA)。EDV 表面設計有特異性結合 T 細胞表面蛋白 CD3 的抗體片段,確保 Cas9 系統能夠精準地遞送至 T 細胞。此外,CD3 的刺激還能誘導 T 細胞增殖,爲後續的同源定向修復提供條件。
其二是腺相關病毒(AAV)載體,它負責攜帶編碼 CAR 蛋白的 DNA,這段 DNA 兩端帶有 T 細胞受體α恆定基因(TRAC)的同源序列。研究團隊還對 AAV 進行了進化,使其能夠規避預存的抗 AAV 抗體,並能通過與 T 細胞和自然殺傷細胞表面的 CD7 蛋白相互作用,特異性地感染 T 細胞。
這項設計的精妙之處在於,一個 T 細胞必須同時接收提供切割工具的 EDV 和提供修復模板的 AAV 這兩種載荷,才能被成功改造爲 CAR-T 細胞。
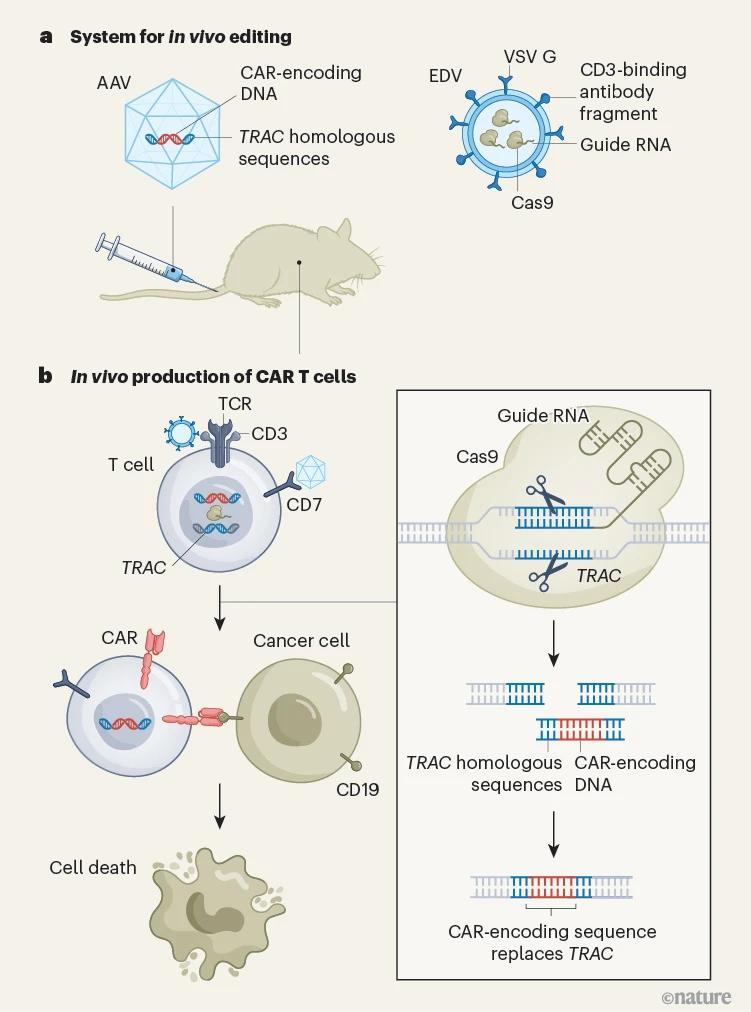
圖 | 體內編輯免疫細胞(來源:Nature)
這種位點特異性插入具有多重優勢,首先是能夠確保 CAR 基因的安全插入,避免隨機插入可能導致的致癌風險。其次,將 CAR 基因插入 T 細胞特有的 TRAC 基因位點,能夠讓 CAR 的表達僅限於 T 細胞,並受到生理性調控,最大限度避開對其他細胞類型的誤編輯。最後,這項技術還避免了 CAR 基因隨機整合後,可能出現的 T 細胞過度激活或耗竭等功能障礙問題。
研究證實,該系統在體外對人 T 細胞的敲入效率顯著提升,在小鼠模型中,CAR 插入和表達幾乎僅限於 CD4+和 CD8+ T 細胞,在自然殺傷細胞、巨噬細胞、造血幹細胞及惡性 B 細胞系中幾乎檢測不到。
更新後,除了能治血液瘤,實體肉瘤也能治了
研究團隊在多個小鼠模型中驗證了這一系統的有效性。這些小鼠被植入了不同類型的人類癌細胞,包括白血病、多發性骨髓瘤和子宮肉瘤。結果令人振奮,在接受治療的小鼠體內,白血病和多發性骨髓瘤細胞被完全清除。
其中,新系統對白血病和骨髓瘤小鼠的療效優於體外製備策略,有部分小鼠還形成了長期免疫記憶,超過一半的肉瘤(實體瘤)小鼠實現了完全緩解。馬爾拉漢醫學研究所的免疫學家雷切爾·佩雷特(Rachel Perret)博士特別指出,此前 CAR-T 治療實體瘤的成功率較低,這一突破的“鼓舞人心”之處還在於,有望推動該療法在實體瘤領域發揮作用。
工程後的 CAR-T 細胞成功表現出增殖與激活特徵,同時保留了幹細胞樣特性,有利於長期存活,研究期間並未觀察到明顯的系統性毒性或體重異常。
目前,艾奎姆已聯合創立了生物技術公司 Azalea Therapeutics,正在猴子身上測試這一方法,計劃於 2027 年年底前啓動人體臨牀試驗,最終實現臨牀轉化。
波士頓大學的合成生物學家 Wilson Wong 博士指出,在這項技術中,大部分治療物質會遞送至 T 細胞,但仍有少量可能進入其他細胞,尤其是肝臟,但他也表示,這項新系統“令人印象深刻”,爲複雜的體內 CAR-T 療法指明瞭方向,“從技術上講,這非常令人興奮。”
儘管這項研究取得了突破性進展,但將該技術推向臨牀仍面臨諸多挑戰。首先,需要進行更深入的研究,以排除可能出現的意外基因修飾,包括對非 T 細胞類型或非 TRAC 基因組位點的脫靶效應。考慮到經過編輯的 T 細胞在組織中廣泛分佈,這項評估將是艱鉅的任務。而且,治療效果能持續多久,以及是否會引入其他不必要的基因組變化,這些都有待進一步觀察。
該技術還存在免疫失調的風險,目前的小鼠模型使用的是健康的 T 細胞,而癌症患者的免疫細胞通常處於功能失調狀態。未來需研究該方法在癌症免疫微環境模型中的效果,以及是否需要結合其他免疫療法來支撐自體合成 CAR-T 細胞的抗腫瘤反應。
此外,經典 CAR-T 療法中的免疫細胞清除預處理,除了爲 CAR-T 細胞騰出空間,還具有減少免疫抑制細胞和改變腸道微生物羣等功能,這些都可能影響 CAR-T 細胞的活性。體內工程化方法無法結合這種預處理,因此需要探索其他免疫調節相關的輔助策略。
儘管存在這些挑戰,這種靶向雙遞送策略,依舊爲體內位點特異性插入治療基因提供了一種令人興奮的可能。這項工作不僅是 CAR-T 細胞療法領域的重大飛躍,更預示着基因編輯技術將以更安全、更高效、更可及的方式,改寫未來醫學的藍圖。
參考文獻:
https://www.nature.com/articles/d41586-026-00857-6
https://www.nature.com/articles/d41586-026-00634-5
https://www.nature.com/articles/s41586-026-10235-x
運營/排版:何晨龍
本文是專業學術論文解讀,不做醫療建議。





