肝臟是人體中再生能力最強的實體器官,能夠在失去 70% 體積後自行修復。然而,當這種令人讚歎的再生能力也不足以對抗疾病時,患者便走到了一條單行道的盡頭:器官移植。
然而,全球每年有數百萬人死於終末期肝病,其中真正能等到合適供體的患者,不過是幸運中的少數。他們在等待移植名單上煎熬,結局卻是因病情過重,最終失去接受移植的機會,或在手術前離世。
幾十年來,肝臟組織工程學者一直試圖在實驗室培育出可供移植的肝臟組織,卻始終無法突破一個核心瓶頸:在植入前將工程化肝組織擴大至具有治療意義的體積。
直到今年 4 月 17 日,在最新發表於《科學進展》(Science Advances)的一篇論文中,哈佛大學懷斯生物啓發工程研究所(Wyss Institute at Harvard University,下文簡稱懷斯研究所)主導的聯合團隊選擇了一條截然不同的路徑:不在實驗室裏解決規模化問題,而是將這項任務“外包”給患者自己的身體。他們結合組織工程學與合成生物學,創造出一種可以在體內遠程接收成長指令的工程化肝臟構建體,並首次在動物實驗中實現了植入後的按需擴增。
器官短缺與組織工程的雙重困境
肝臟一旦病變至終末期,此前強大的自我修復能力就徹底崩潰。此時,肝臟移植是唯一的治癒性手段。然而,供需之間的鴻溝使這一選項對許多患者來說近乎奢望。
理論上,組織工程學提供了一條有吸引力的替代路徑:在實驗室培育出功能性的工程化肝組織,作爲等待移植的“橋樑”,甚至有望在未來直接替代移植。過去數十年,研究人員在三維生物打印、血管化構建、細胞封裝等技術上取得了大量進展,已經有能力培育出在短期內具備基本代謝功能的工程化肝組織構建體。
然而,這一領域面臨着一個始終未被突破的根本性瓶頸:可植入工程化肝組織的最大尺寸依然有限,與提供有意義的治療所需的體積之間存在數量級的差距。這一問題並非肝臟獨有,工程化心臟、腎臟、肌肉等組織無一例外地受到同樣的規模上限約束。
這種規模化困境來自三重技術障礙。其一是細胞來源問題,很難獲取足夠數量高質量的原代人類肝細胞(hepatocytes,HEPs)構建大體積構建體;其二,在密集堆積的三維組織中,細胞的氧氣與營養物質供應需求巨大,需要與之相匹配的血管化網絡;其三,將大量細胞以保持活性的方式組裝成大尺寸三維結構,在工藝上至今沒有可靠解決方案。三維生物打印、類器官培養、去細胞化再細胞化、生物反應器設計等方向均在推進,但均未能徹底解決上述問題。

圖 | 克里斯托弗·陳(Christopher Chen)和桑吉塔·巴蒂亞(Sangeeta Bhatia)(來源:Wyss Institute at Harvard )
面對這一困境,懷斯研究所的克里斯托弗·陳(Christopher Chen)教授聯合桑吉塔·巴蒂亞(Sangeeta Bhatia)教授領導的研究團隊,決定重新審視框架本身。他們想到,是否可以先植入一個小規模的工程化肝組織構建體,在其成功定植於宿主體內之後,再通過外部給藥的方式驅動它在體內自發擴增?如果成功,一個擴增後功能完整的“衛星肝臟”,便可以立即分擔受損肝臟的代謝負荷,爲患者等待供體器官贏得寶貴的時間窗口。
BOOST 策略:思路、設計與工作原理
研究團隊將這一策略命名爲“BOOST”,全稱爲“基於合成生物學觸發的生物工程按需外擴生長”。這一思路將工程難題轉化爲生物學控制問題,利用人體成熟的血管網絡解決營養供應,再利用合成生物學解決生長控制。
BOOST 策略的核心邏輯分爲兩個層次:第一,識別並破解驅動緻密三維肝組織中肝細胞增殖所需的關鍵生物學信號組合;第二,通過合成生物學工具,將這些信號的“開關”安裝在工程化肝組織細胞的基因線路中,使其可以在外部給藥的觸發下精確、可逆地啓動。
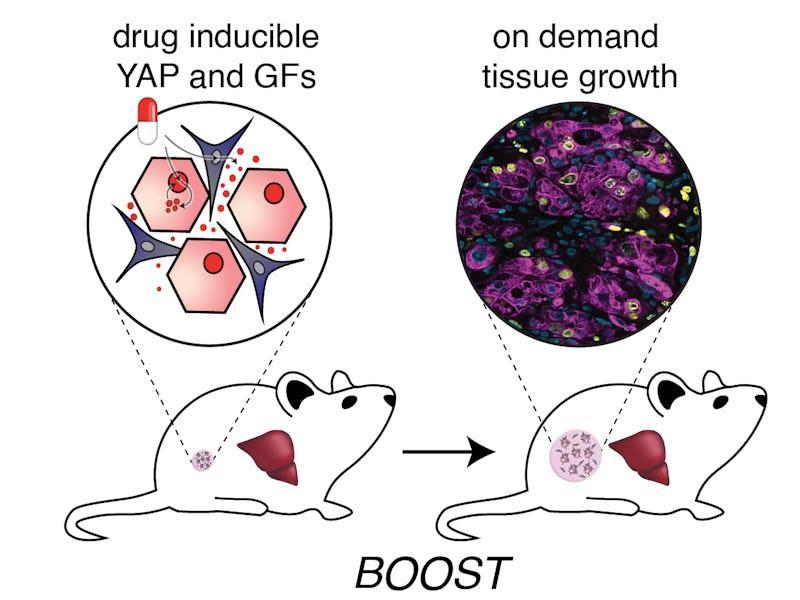
(來源:Wyss Institute at Harvard University)
肝臟的再生生長由多種可溶性生長因子(GFs)調控。研究團隊以原代人類肝細胞(HEPs)爲模型,系統篩選後,最終確定了四種關鍵因子:HGF、TGFα、WNT2 和 RSPO3。
其中,肝細胞生長因子(HGF)是肝再生的經典調控分子,可促進細胞分裂;轉化生長因子α(TGFα)促進肝細胞增殖;WNT2 同樣參與肝細胞命運決定和增殖,R-脊椎蛋白 3(RSPO3)則是 WNT 信號通路的增強子,負責放大信號。
然而,當研究人員將這四種生長因子應用於高密度 HEPs 和成纖維細胞組成的三維肝組織時,效果卻大打折扣。這次挫折使研究人員意識到,緻密組織中可能存在額外的增殖抑制機制。
他們隨後將目光轉向一個名爲 Yes 相關蛋白(YAP)的胞內蛋白。YAP 是 Hippo 信號通路的核心下游效應因子,具有感知細胞密度等機械信號,參與細胞密度調控的能力。在肝臟發育、穩態維持和病理過程中扮演着複雜的多重角色。這意味着,即便存在外源性生長因子,細胞密度本身也會通過 YAP 降解阻斷了增殖信號。
爲突破這一增殖限制,研究者在 HEPs 中引入了一種經過改造的、不可降解的 YAP 突變體: 這種突變體能無視細胞間的機械壓力,強制進入細胞核參與基因調控,從而繞過了密度感知的增殖檢查點。實驗進一步證實,只有非降解型 YAP 與前述四種特定生長因子協同作用時,密集的人類肝細胞才能實現強力擴增,五種元素缺一不可。
近一個世紀以來的肝再生研究主要基於動物模型,而 BOOST 的前期工作證實,人類肝細胞增殖有其獨特的調控邏輯,比僅從齧齒動物中獲得的認知更爲複雜。
明確驅動密集肝組織增殖所需的信號組合之後,研究團隊面臨的下一個挑戰是:如何將對這些信號的控制權安裝到工程化細胞的內部,使其可以在體內按需啓動和關閉?
這時,就輪到合成生物學工具發揮作用了。研究團隊分別改造了兩類細胞:首先將四種生長因子分別編碼至不同的成纖維細胞系,使各系細胞能分泌其中一種生長因子。這一改造使得原本只作爲支撐性細胞存在的成纖維細胞,額外承擔了“生長因子供給者”的角色。此外,研究人員還在 HEPs 中引入了不可降解型 YAP 突變體的表達盒。
接着,團隊將以上所有蛋白的表達置於多西環素(DOX)誘導啓動子的控制之下。DOX 是一種常用的廣譜抗生素,在臨牀醫學和基礎研究中均有廣泛的安全使用記錄。這套系統也是分子生物學領域經典且成熟的基因調控工具。
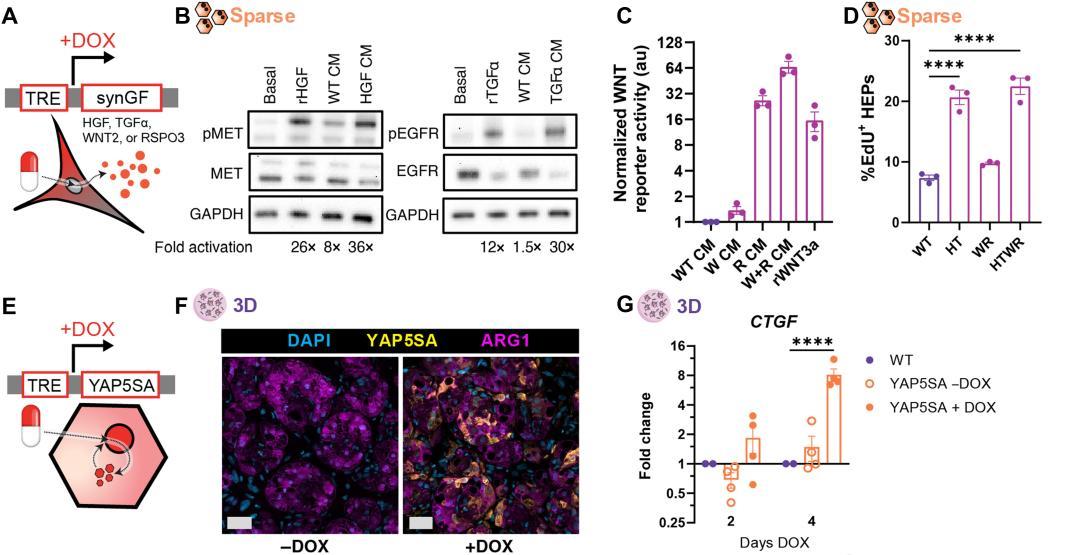
(來源:DOI: 10.1126/sciadv.adz8362)
在體外時間進程實驗中,研究團隊確認,改造後的三維肝組織在持續 7 天的 DOX 處理下實現穩步擴增,組織的體積和細胞數量均顯著增加;只有當 DOX 存在時,生長程序纔會啓動,一旦停藥,蛋白合成即刻停止,HEPs 的增殖活動也隨之停止。
值得注意的是,對單細胞基因表達的分析顯示,在高增殖狀態下,HEPs 的功能狀態下降。研究團隊也給出瞭解釋,這是在多種生物學場景中廣泛存在的“增殖-分化權衡”,是細胞生物學的一種自然現象。他們同時指出,未來或許可以利用肝臟的原生再功能化信號,恢復植入肝細胞的功能狀態。
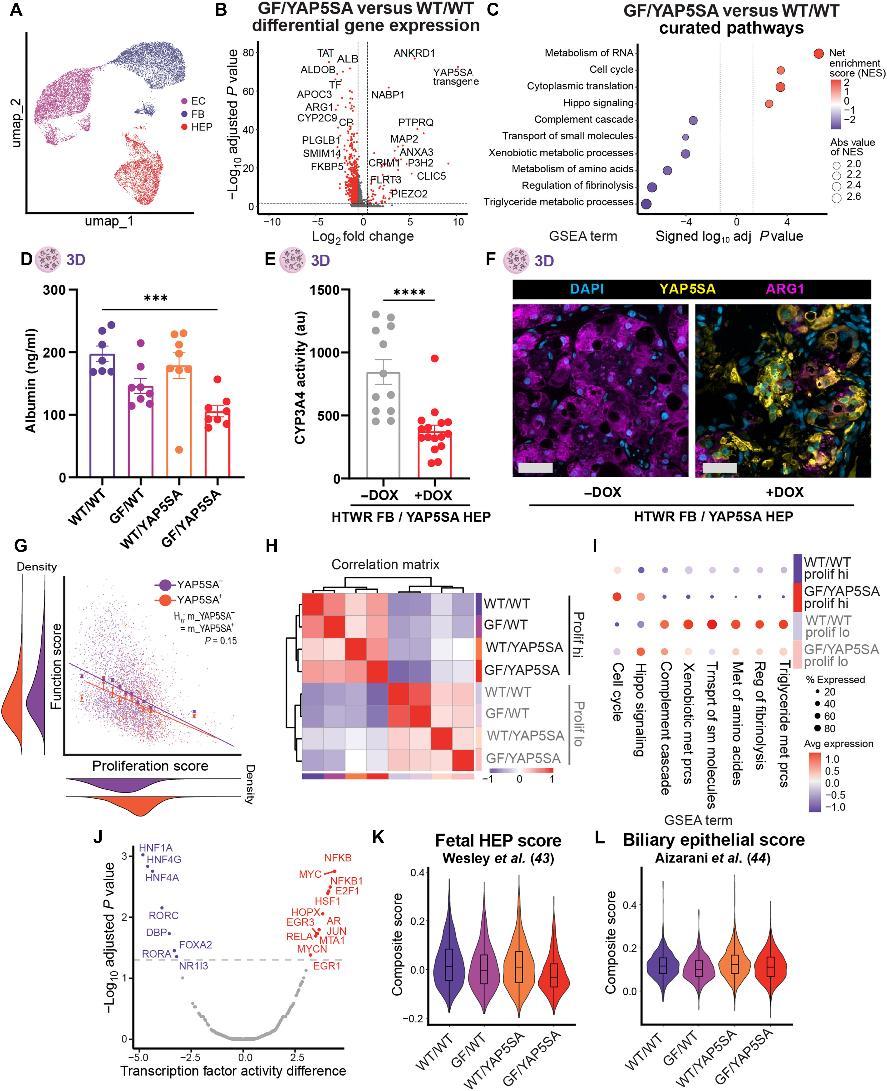
圖 | YAP/GF 擴增的 HEP 保持分化細胞狀態,並在功能和增殖之間表現出權衡。(來源:DOI: 10.1126/sciadv.adz83)
植入小鼠體內的在體擴增驗證
體外驗證之後,要想讓這套系統真正走向臨牀,研究人員還需要證明,在活體宿主體內植入 BOOST 工程化肝組織構建體,其能否實現相應的擴增響應。爲此,他們將小型 BOOST 工程化肝組織構建體植入免疫功能正常的小鼠體內,待其成功定植後,對小鼠進行與體外實驗相同的 7 天 DOX 系統性給藥。
結果令人振奮,植入的組織在 DOX 給藥期間,增殖率提升約 500%,工程化 HEPs 數量實現了倍增。此外,擴增後的組織自發形成了供血管網絡,支持擴增組織的代謝需求,這是功能性組織存活的必要條件,也說明宿主的血管形成程序被有效激活。
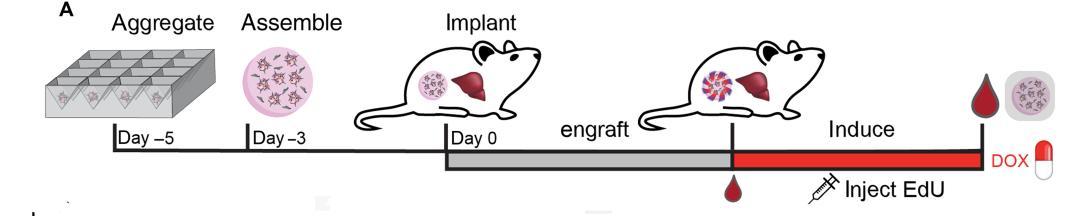
圖 | 活體異位肝組織移植組裝和植入示意圖。(來源:DOI: 10.1126/sciadv.adz8362)
在安全性方面,小鼠在實驗過程中並未出現任何纖維化跡象(通常由免疫細胞侵襲和成纖維細胞炎症反應導致),也未觀察到腫瘤生成。可控的增殖並未觸發致癌過程,這對一種未來具有臨牀應用潛力的策略而言至關重要。
這項研究在更宏觀的座標系中意味着什麼
在此前的肝臟再生策略中,肝細胞的誘導植入和增殖均依賴於宿主肝臟的預先損傷:通過製造一定程度的組織損傷,爲植入細胞創造一個增殖性的生態位,再向宿主肝臟注射生長因子或轉錄因子,刺激再生。
這類策略不僅需要以宿主自身的損傷作爲前提,還面臨遞送效率低、靶向性差、難以精密時序控制等問題,臨牀轉化的可行性存疑。而在 BOOST 研究中,研究團隊在完全健康的宿主中成功誘導了植入組織的在體擴增,完全擺脫了對宿主肝損傷的依賴。
也曾有學者探索,直接注射遊離的人類肝細胞是否可行,但最終在臨牀上宣告失敗。原因在於,注射細胞的植入效率極低,難以在體內形成穩定的功能性組織。事實上,BOOST 的思路更接近於 CAR-T 細胞療法在液體腫瘤領域的應用:先將經過基因改造的細胞(或細胞構建體)植入患者體內,再通過外部信號對其活性進行精密調控。
研究成果雖然令人振奮,BOOST 在當前階段的侷限性也應當被正視。首先,如前所述,處於高增殖狀態的工程化 HEPs 表現出肝臟特異性功能基因表達水平的下調。這意味着,在擴增期間,工程肝組織作爲代謝功能單元的效能可能暫時降低。研究團隊希望,未來通過利用肝臟自身的再功能化信號來解決這一問題。
此外,目前的所有體內實驗均在小鼠模型中進行,且尚未專門在肝病動物模型中驗證 BOOST 組織是否能有效“拯救”受損宿主的肝功能,這將是下一階段至關重要的驗證實驗。從小鼠到靈長類動物再到人類的跨物種推廣,還需要大量額外的安全性和有效性數據。
作爲誘導劑,多西環素雖是已被廣泛批准使用的廣譜抗生素,概念驗證也是清晰的。然而其向人體全身給藥可能帶來的菌羣影響、以及長期應用的潛在副作用,均需在臨牀轉化路徑中予以評估。
現有研究也提示,其在較高濃度下可能影響線粒體功能、細胞代謝等,因此,在向人體臨牀轉化的過程中,替代性可誘導系統(如使用植物來源的激素模擬物或其他誘導劑)的開發將是需要認真考慮的問題之一。
值得注意的還包括基因改造細胞的安全性。BOOST 策略涉及對原代人類肝細胞和成纖維細胞進行穩定的基因改造,引入不可降解 YAP 突變體和生長因子表達盒。在人體應用中,異常增殖的長期安全性監控、基因整合的潛在位置效應等,均需要長期安全性研究。
最後,目前實驗使用的是原代人類肝細胞,其來源本身受限於供體器官的可及性。未來若能與誘導多能幹細胞(iPSC)來源的肝細胞相結合,則可在理論上實現無限細胞來源,但 iPSC 來源 HEPs 的成熟度和功能性尚屬於前沿且較有爭議的研究方向。
更廣闊的應用圖景
除了對抗重症肝臟疾病,BOOST 的意義還在於其爲“按需可控的實體器官細胞療法”這一概念建立了初步的技術原型。
桑吉塔·巴蒂亞教授表示,這一策略的底層邏輯在原理上可以延伸至其他同樣受規模化挑戰困擾的工程化組織療法,例如工程化心肌組織以治療心力衰竭、工程化胰島素分泌組織治療糖尿病等。在這些場景中,能夠先植入小規模的功能性構建體、再按需擴增至治療劑量,將從根本上改變實體器官細胞療法的開發邏輯。
懷斯研究所的創始主任、器官芯片技術的先驅人物唐納德·英格伯(Donald Ingber)教授評價稱,這項研究代表了一種解決移植肝臟供體短缺的全新方案,並具有同等重要的跨疾病應用潛力:“這正是懷斯研究所工作理念的生動體現,我們致力於改變那些往往已別無選擇的患者的生活。”
參考來源:
https://www.science.org/doi/10.1126/sciadv.adz8362
https://wyss.harvard.edu/news/growing-liver-tissue-on-demand-directly-in-the-body/
運營/排版:何晨龍





