

(綜合中國新聞網、央廣網、《合肥日報》)
華盛頓大學蛋白質設計研究所DavidBaker領導的研究團隊,在計算機深度學習技術的幫助下,首次成功設計出多種高效的人造絲氨酸水解酶。與過去的方法不同,這些新設計的酶不再侷限於已有的天然蛋白質結構,而是從頭開始,通過人工智能技術量身定製,突破了以往設計的侷限性。相關成果發表在2025年4月18日出版的Science上。
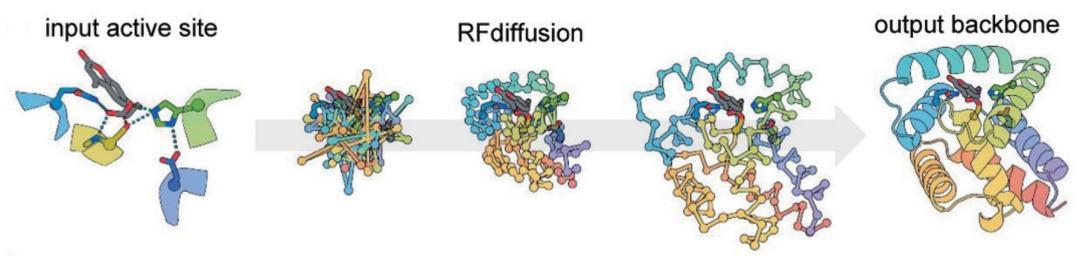
絲氨酸水解酶是一類重要的天然酶,它們在生物體內催化多步複雜的化學反應,具有嚴格精密的催化活性中心,這使得通過計算設計出具有同樣功能的人造酶一直極具挑戰。研究人員利用先進的蛋白質生成模型RFdiffusion,從零開始構建蛋白質骨架,再通過深度學習方法PLACER精確篩選和評估催化反應每一步的結構匹配性,大幅提高了設計成功率。
研究團隊共設計了800多個候選酶,其中多個新酶經實驗驗證表現出顯著的催化活性和結構精確性,最佳催化效率(kcat/Km)達2.2×105M-1·s-1,較此前最強人工設計酶OE1(2018年報道,經4輪定向進化後爲3190M-1·s-1)提升近70倍。同時,晶體結構分析也證實這些新酶的實際構型與計算模型高度吻合,精度達到原子級別。更重要的是,其中5種酶採用了自然界從未出現的全新摺疊,爲未來定製催化器件打開了額外的結構空間。
這項突破性的研究不僅實現了人工酶設計領域的重大跨越,也爲未來設計其他多步催化的複雜酶類奠定了方法基礎。儘管這些人工酶與天然“頂尖選手”——如乙酰膽鹼酯酶仍有差距,但其性能已達到甚至超過多數工業酶的實用區間,展示了巨大的應用潛力。
(來源Science)
《科技導報》創刊於1980年,中國科協學術會刊,主要刊登科學前沿和技術熱點領域突破性的成果報道、權威性的科學評論、引領性的高端綜述,發表促進經濟社會發展、完善科技管理、優化科研環境、培育科學文化、促進科技創新和科技成果轉化的決策諮詢建議。常設欄目有院士卷首語、智庫觀點、科技評論、熱點專題、綜述、論文、學術聚焦、科學人文等。






