本文是專業學術論文解讀,不做醫療建議。
自上世紀 90 年代抗逆轉錄病毒治療(ART)問世以來,艾滋病病毒(HIV)感染已從一種致命性疾病轉變爲可通過服藥有效控制的慢性病。患者只要堅持服藥,血液中的病毒水平可被抑制至檢測不到的程度,從而享有正常的生活和壽命。然而,這並非真正的治癒,因爲一旦停藥,患者的體內病毒會在數週內迅速反彈,重新佔據主導地位。
這一頑固復發現象的背後,是一個困擾科學界近三十年的核心難題——HIV 的“潛伏感染”。病毒會將自己的遺傳物質整合到極少數免疫細胞的基因組中,並進入一種休眠狀態,這些細胞如同深埋地下的“病毒保險箱”,在抗病毒藥物的壓力下保持沉默,伺機而動。
這些攜帶完整、有複製能力病毒的細胞羣體,被稱爲“病毒庫”。由於其數量極其稀少——在患者每一百萬個 CD4+ T 細胞中可能僅有 1 到 100 個,科學家長期以來難以捕獲並深入研究它們,根除病毒庫的目標遙不可及。
近日,發表在 Nature 上的一項研究在這個問題上取得重大突破, 文章以加速預覽(Accelerated Article Preview)形式發表。來自康奈爾醫學院、洛克菲勒大學等機構的研究團隊,成功分離並培養出能夠長期存活、持續產生感染性病毒的免疫細胞克隆。這些被稱爲“真實病毒庫克隆”(ARCs)的細胞,讓科學家第一次能在實驗室中近距離觀察 HIV 最頑固的藏身之所。

圖 | 團隊論文:HIV 儲庫克隆中的抗原動態表達和細胞毒性 T 細胞耐受性(來源:Nature)
在實驗伊始,研究團隊面臨的最大挑戰是如何從海量細胞中找到這些稀有的“帶毒者”。團隊改進了篩選技術,通過特定的免疫標記將可疑細胞富集,並利用 HIV 蛋白作爲檢測探針。只有真正產生病毒的細胞纔會被保留,經過反覆純化,最終獲得了純度接近 100% 的病毒庫克隆。
令人意外的是,在放入含有抗病毒藥物的培養基中,這些細胞不僅沒有死亡,反而能夠穩定增殖,在體外存活數月並擴增到數億個。這打破了過去只能從患者血液中短暫觀察病毒庫細胞的侷限,爲深入研究提供了充足的材料。整個研究共分離出 10 個這樣的克隆,其中 7 個攜帶完整的 HIV 基因組,3 個攜帶缺陷病毒。
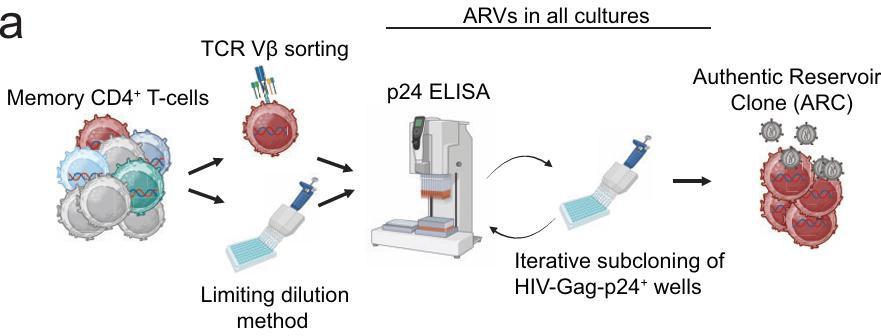
圖 | 真實病毒庫的分離策略及過程(來源:論文)
通過基因測序,研究團隊揭示了一個重要規律:在 7 個完整病毒中,有 6 個整合在人類基因組中轉錄活性較低的“冷區”(cold spot),如鋅指蛋白基因或異染色質區域。相比之下,缺陷病毒更多整合在普通基因中。
團隊判斷這並非偶然。病毒最初感染時的整合位置是隨機的,但在長期的免疫壓力下,那些整合在活躍基因區的病毒更容易被激活表達,從而暴露給免疫系統被清除;而藏身於冷區的病毒則能更好地保持沉默,在患者體內存續多年。這就像是一場長達數年的捉迷藏比賽,最終獲勝的都是最擅長隱藏的選手。
研究團隊對一位代號爲 OM5334 的患者進行的 12 年追蹤印證了這一點。在抗病毒治療初期,患者體內總的病毒庫迅速衰減,但三個特定的克隆卻保持了驚人的穩定。治療開始時它們各佔感染細胞的比例不到 0.2%,但 3.5 年後,其中一個克隆竟佔到了所有完整病毒庫的 34.6%。
進一步的分析揭示了這些“長壽”克隆的祕密武器。研究發現,這些細胞屬於一類特殊的記憶 T 細胞,它們擁有針對 EB 病毒的免疫應答能力。
EB 病毒是一種常見的皰疹病毒,在全球超過 90% 的成年人體內潛伏着。這意味着,這些攜帶 HIV 的 CD4+ T 細胞實際上是在“寄生”於人體正常的免疫反應中。
每當人體需要調動免疫系統來對抗 EB 病毒等其他病原體時,這些潛伏的 HIV 克隆細胞也會被一同激活並開始大量增殖,以支持針對外來威脅的免疫應答。在這個過程中,它們不僅實現了自身的複製,還順帶維持了 HIV 的潛伏感染狀態,可以說一舉兩得。這種巧妙的增殖模式,使得病毒庫的規模能夠在一定程度上自我維持甚至擴大,極大地增加了清除的難度,也解釋了爲何病毒庫一旦形成就如此難以衰減。
在傳統的“激活—殺傷”治療策略設想裏,如果能用藥物強制激活潛伏的病毒,讓感染細胞暴露出來,免疫系統就能將它們清除。但研究表明,現實並非完全如此。在未受刺激的狀態下,不同病毒庫克隆中只有 0% 到 3.4% 的細胞表達病毒蛋白。而且即使用被認爲能“最大程度”激活 HIV 的強力刺激劑處理,大多數病毒仍頑固地保持沉默。
深入分析揭示,雖然刺激能啓動病毒基因的轉錄,但大部分轉錄過程會在中途受阻,無法產生完整的病毒蛋白。這完全顛覆了簡單“激活—殺傷”策略的理論基礎。
既然有些細胞確實在表達病毒蛋白,爲什麼免疫系統不能將它們清除?研究團隊設計了一種“慢速治癒”實驗,讓 HIV 特異性的細胞毒性 T 淋巴細胞(CTL,主要職責是直接識別並消滅被病毒感染的細胞、癌細胞或受損細胞)與病毒庫細胞共同培養。
研究發現,病毒庫細胞對免疫清除的反應存在巨大差異。對於像 ARC-ZNF721 這樣“脆弱”的克隆,即使它們極少表達病毒(瞬時表達率<2%),只要 CTL 免疫殺傷力足夠強且持續時間長,就能通過累積效應清除超過 90% 的細胞。
然而,另一類像 ARC-Chr16 的克隆卻天生帶有“護甲”,即便在同樣的免疫壓力下不僅未被清除,反而持續擴增。實驗證實,這種抗性並非來自病毒本身,而是源於細胞自身的代謝特性:它們擁有極低的氧化應激水平,能有效抵禦 CTL 攻擊時引發的致命“氧化風暴”。
針對這一機制,研究提出了“代謝增敏”的全新策略。團隊發現,使用一種已獲批的老藥去鐵胺(DFO)可以提高這些耐藥細胞內的氧化應激水平,強行將其推過“死亡閾值”,使其重新對 CTL 殺傷敏感,從而將病毒釋放量降低了 95% 以上。
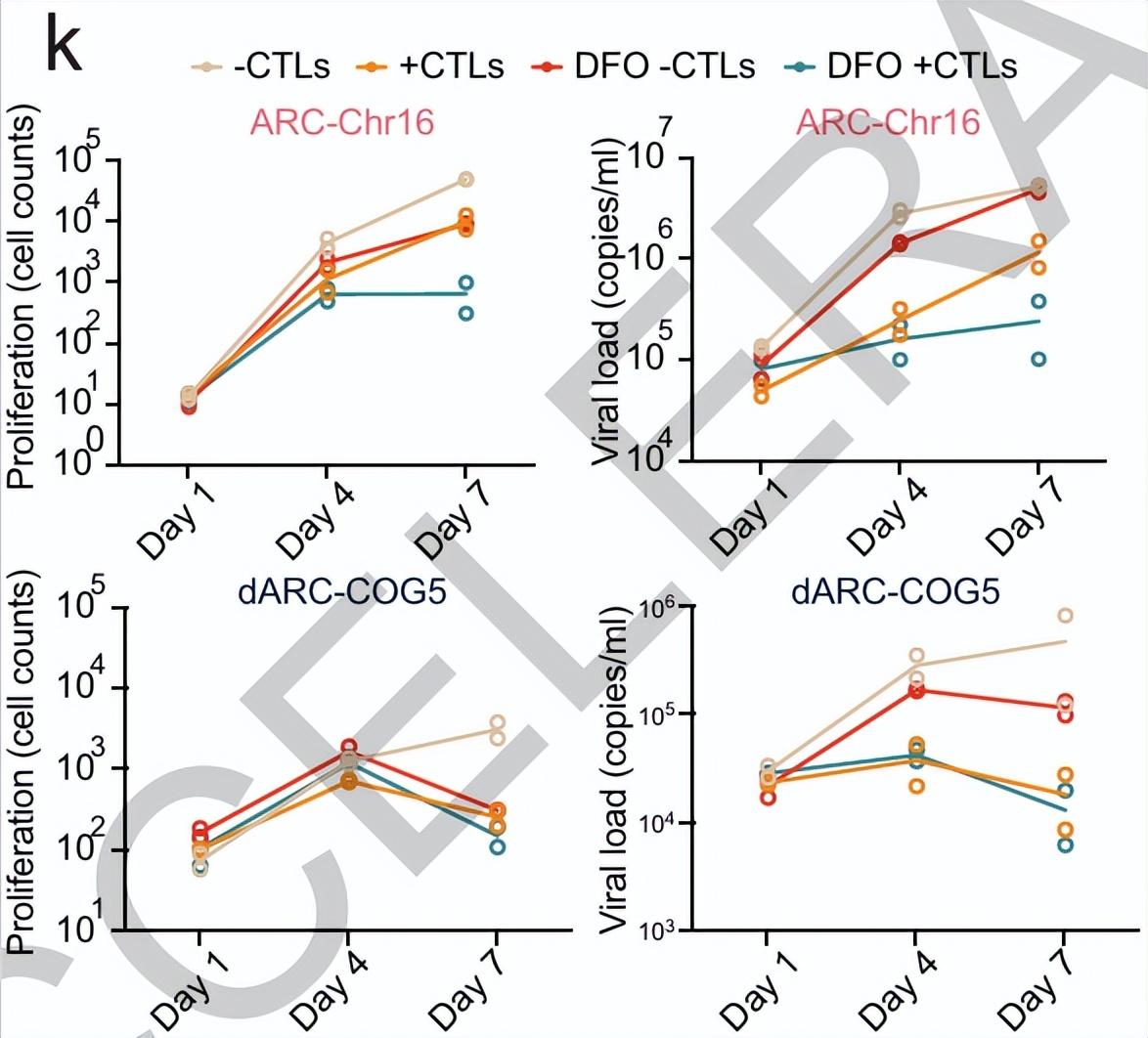
(來源:論文)
此外,研究還指出患者體內的免疫細胞常因長期對抗病毒而“疲憊”(缺乏殺傷性顆粒酶 B),可通過免疫因子 IL-15 恢復其功能。
總的來說,這項研究爲 HIV 治癒繪製了一幅比以往更清晰的圖景。病毒庫細胞並非鐵板一塊,而是展現出高度異質性:有的深藏在基因組冷區,有的對免疫殺傷敏感,有的則具有內在抗性。這意味着,未來的治癒方案可能需要“三管齊下”:用藥物削弱病毒庫的代謝防禦、喚醒疲憊的免疫系統,並配合持續的免疫壓力,纔能有效清除這些頑固的病毒庫。
從治療角度看,DFO 作爲已上市藥物,其增敏免疫殺傷的作用提供了最直接的臨牀應用線索。但將一種鐵螯合劑重新定位用於 HIV 治療,仍需要解決劑量、給藥方式和全身副作用等問題。
當然,研究也存在明顯侷限。病毒庫克隆的分離方法本身可能存在選擇偏向,傾向於捕獲那些會表達病毒且表達後不會立即死亡的細胞。此外,長期體外培養可能改變細胞的某些狀態。研究團隊坦承,要驗證這些克隆是否真正代表導致復發的主要病毒庫,還需要與臨牀治療中斷研究相結合。
參考鏈接:
論文 DOI:
https://doi.org/10.1038/s41586-026-10298-w
運營/排版:何晨龍
本文是專業學術論文解讀,不做醫療建議。





