本文是專業學術論文解讀,不做醫療建議。
視網膜母細胞瘤(RB)是兒童最常見的眼內惡性腫瘤,在大多數患者中,視網膜母細胞瘤僅限於眼部,通過早期檢測和可用治療,該癌症的治癒率超過 95%。但如果該疾病未得到及時治療,它可能擴散到身體的其他部位,此時會很難治療。
目前主要治療方式包括玻璃體內注射、放射治療、冷凍治療和全身化療,通常會導致嚴重的眼部結構損傷和全身毒性。此外,有眼外擴散風險的患者通常需要進行眼球摘除術,從而導致永久性視力喪失。
醫學界一直渴望開發一種無創治療,不用打針、不用手術,滴眼藥水就能把藥送到眼底。但眼睛有天然的防護屏障,包括角膜上皮、血視網膜屏障等,常規眼藥水 99% 無法穿透,藥物根本到不了眼底病竈。
2025 年發表的多篇綜述文章指出,非侵入性(主要是局部眼藥水)眼底藥物遞送面臨巨大挑戰:滲透率低(通常<5%)、屏障機制複雜、安全性問題、機制爭議等。
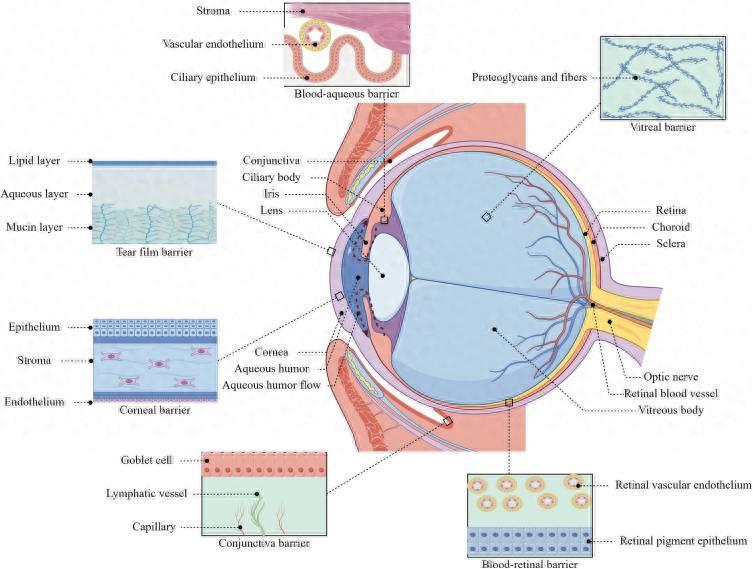
圖 | 藥物在遞送過程中面臨多種挑戰(來源:參考鏈接[2])
近日,來自瀋陽藥科大學的研究團隊在 Science Advances 發表研究成果,他們證明,利用從豬精液中提取的外泌體搭載抗癌藥物,可以眼藥水形式滴進眼睛,穿過層層眼部屏障,直達視網膜深處。在小鼠 RB 模型中,這種眼藥水不僅顯著抑制了腫瘤生長,還完美保住了視網膜功能,讓小鼠的視力電生理測試幾乎恢復正常。
外泌體是細胞分泌的納米級 “小泡”,由於其良好的生物相容性、低免疫原性以及穿越生物屏障的能力,已成爲極具前景的藥物遞送候選者。
在精子向卵子長途跋涉的遷移過程中,精液中的外泌體扮演着至關重要的角色。它們不僅能釋放免疫抑制因子爲精子披上“隱形斗篷”,避免遭到女性生殖道免疫系統的清除;還能利用表面攜帶的特定功能蛋白,短暫地打開生殖道上皮細胞間的緊密連接,協助精子順利突破黏液與細胞等物理屏障。此外,外泌體在沿途會不斷與精子融合,爲其補充關鍵的蛋白質、脂質和抗氧化物,在抵禦氧化損傷的同時,促使精子發育成熟、獲得運動能力並最終完成受精所需的“獲能”。
也正是這一特性,讓團隊不禁思考,這些顆粒是否也能穿過眼部的屏障。
他們從杜洛克豬精液中提取了外泌體,並在外泌體內部裝載了一種特殊的“納米酶系統”,包含碳點、二氧化錳和葡萄糖氧化酶,做成了 FA-SEVs@CMG 眼藥水。
爲了提高靶向選擇性,研究人員在精液外泌體表面修飾了葉酸分子,因爲視網膜母細胞瘤的癌細胞表面有大量葉酸受體,這能讓外泌體只識別癌細胞,不傷正常眼細胞,避免誤傷,實現精準靶向。
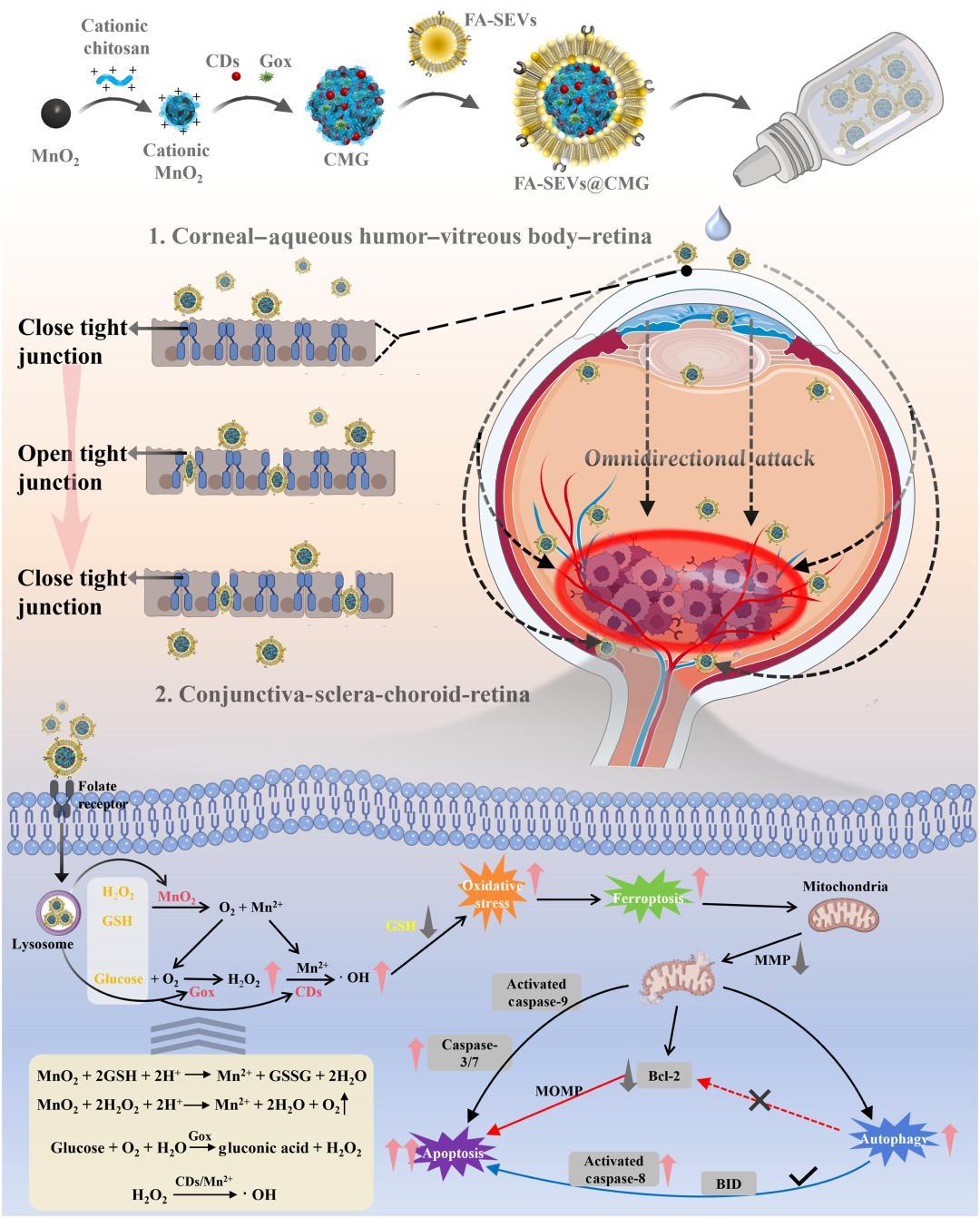
圖 | FA-SEVs@CMG 在視網膜母細胞瘤中的治療作用示意圖(來源:上述論文)
爲了驗證 FA-SEVs@CMG 眼藥水的有效性和安全性。研究人員做了大量實驗,從體外細胞到小鼠、兔子模型。
在細胞實驗階段,研究人員分別將藥物作用於正常眼細胞和視網膜母細胞瘤細胞。結果顯示,即便在較高濃度下,角膜細胞、視網膜細胞、晶狀體細胞等正常組織依然保持高度活性,存活率超過 85%,說明藥物對眼睛本身非常安全。而面對癌細胞時,藥物展現出強大的殺傷能力,抑制率達到 82.7%,遠優於單純藥物和普通載體組。
通過熒光標記追蹤可以清晰看到,帶有葉酸“導航”的藥物大量聚集在癌細胞內部,而在正常細胞中分佈極少,靶向效果直觀可見。進一步機制檢測證實,藥物進入癌細胞後,迅速消耗葡萄糖使其“斷糧”,同時清除癌細胞的抗氧化防禦,引發劇烈的氧化應激反應,最終觸發鐵死亡通路,讓癌細胞走向不可逆的死亡,而不會引起正常組織的損傷。
此外,研究團隊還採用離體豬角膜模型,模擬人眼的真實屏障結構,測試了FA-SEVs@CMG 的穿透效率。數據顯示,普通藥物 10 小時內的角膜穿透率僅有 2% 左右,普通外泌體載體也僅有不到 6%,而這款新型滴眼劑的穿透率達到 14%,是普通藥物的 7 倍、普通外泌體載體的 2.4 倍,並且在 6 小時左右就能達到濃度峯值。
在活體動物安全性實驗中,研究團隊選用兔子,連續多天進行滴眼處理。觀察發現,動物眼表沒有出現紅腫、炎症、分泌物增多等異常現象,角膜保持透明,視網膜結構完整,沒有出現明顯的細胞凋亡或組織損傷,體內肝腎功能指標也均在正常範圍,證明長期局部用藥不會帶來明顯的全身或局部毒性。
最後,研究人員在眼癌小鼠模型上進行了測試。30 天后,腫瘤體積縮小 60% 以上,生長完全受抑,視網膜結構完整、功能正常。而那些使用含有納米酶系統成分但未包裹在外泌體中的滴眼液的對照組小鼠,腫瘤則繼續生長,並擴散到眼睛的其他部位。
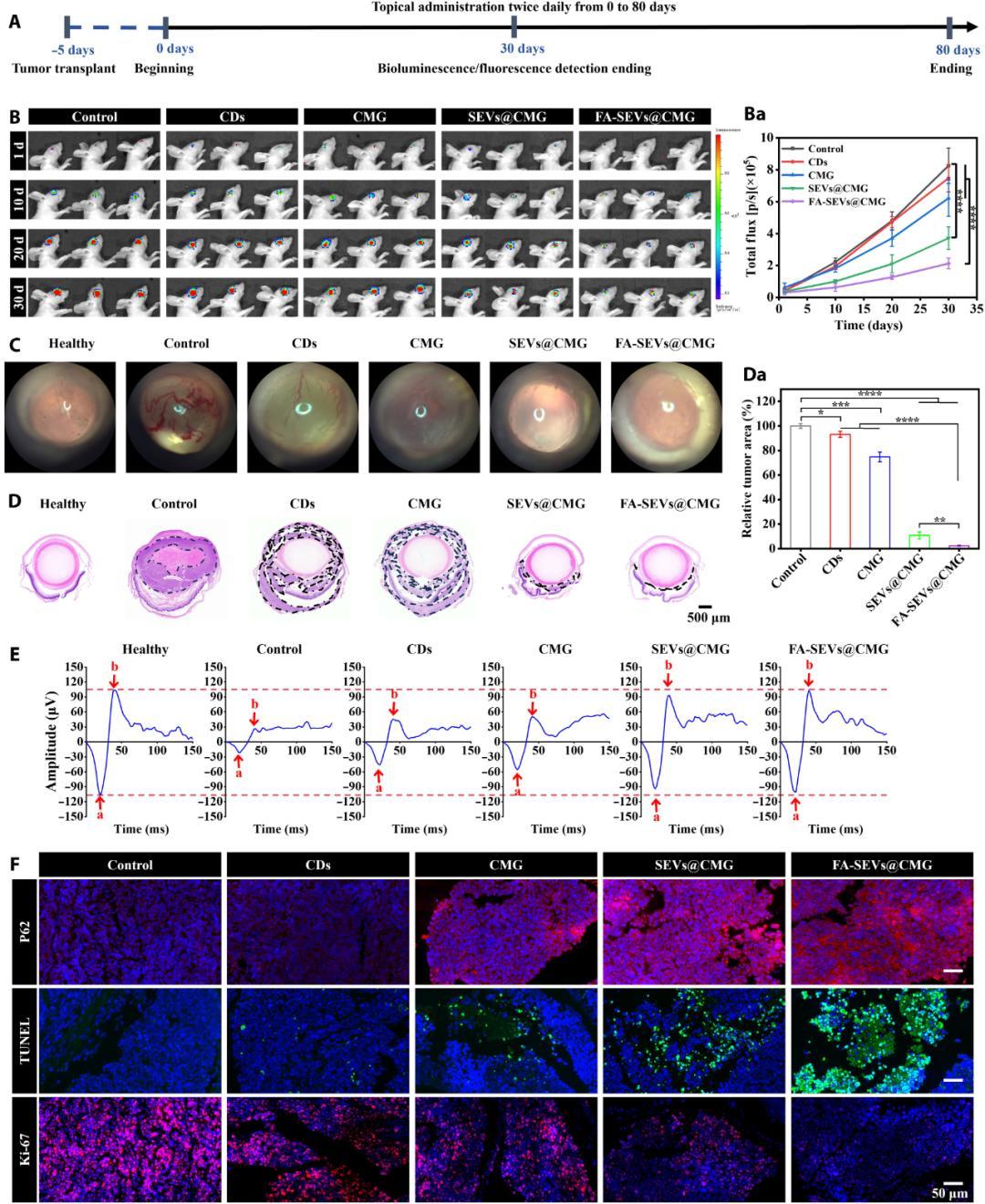
圖 | FA-SEVs@CMG 在 RB 小鼠體內的藥效學研究(來源:上述論文)
進一步的研究發現,FA-SEVs@CMG 能滲透到眼底的機制在於,豬精液外泌體表面天然富含的 EGF 樣蛋白,可作爲關鍵信號分子,直接激活角膜上皮屏障細胞表面的 EGFR 受體,進而啓動下游一系列信號激活,促使細胞骨架發生適度收縮,使得構成眼部屏障的緊密連接蛋白出現暫時性、可控性解聚與重排,在不損傷細胞結構的前提下爲藥物打開通道。最關鍵的是,該通道會在 23 小時內自動恢復,完全可逆。
澳大利亞阿德萊德大學研究藥物輸送和納米醫學的研究員 Chunxia Zhao表示,這項技術可以改善藥物穿過其他類似難以突破的屏障,例如血腦屏障,用於治療包括阿爾茨海默病在內的疾病,或黏膜屏障的輸送。但她表示,另一個未知數是,開發這種液滴所需的複雜系統是否可以大規模生產。
澳大利亞墨爾本貝克心臟與糖尿病研究所的生物醫學和分子蛋白質組學研究員 David Greening(大衛·格林寧)表示,滴眼液形式的藥物比眼內注射藥物的侵入性更小。但他指出,這項研究目前只是概念驗證,還需要進行人體試驗。
研究團隊在論文中指出,這種基於豬精液外泌體的眼部遞藥系統具有很強的通用性,未來不僅可用於視網膜母細胞瘤,還計劃研究其在威脅視力的視網膜病變中的更廣泛治療潛力,包括新生血管性年齡相關性黃斑變性和增殖性糖尿病視網膜病變。
參考鏈接:
1.https://www.science.org/doi/10.1126/sciadv.adw7275
2.Lin, X., Zhou, Y., Lv, K., Wu, W., & Chen, C. (2025). Nanomedicine-Based Ophthalmic Drug Delivery Systems for the Treatment of Ocular Diseases. International journal of nanomedicine, 20, 9221–9249. https://doi.org/10.2147/IJN.S532074
3.Ye, Y., Zhang, Y., Zhao, P., Shen, Y., Hu, P., Wang, L. and Long, D. (2025), Delivery Routes of Topical Eyedrops Reaching the Posterior Segment of the Eye-Recent Advances. Chem. Eur. J., 31: e02324. https://doi.org/10.1002/chem.20250232
排版:胡莉花
本文是專業學術論文解讀,不做醫療建議。





