假如細胞也有“年輪”,那科學家會不會更容易讀懂生命歷史?一項最新研究正在將這種設想轉變爲現實。
美國約翰斯·霍普金斯大學林鼎昌教授團隊與諾獎得主、美國華盛頓大學 David Baker 教授合作,開發了一種基因編碼的細胞內“記憶體”GEMINI(Granularly Expanding Memory for Intracellular Narrative Integration),來回溯每個細胞的歷史。
開發 GEMINI 的思路是把“時間”帶回固定樣本:研究團隊設計了一種細胞內蛋白自組裝作爲信息的讀寫載體,在自組裝過程中,可以將胞內信號以熒光條帶的形式持續寫入。
通過引入“時間戳”,這些信息可以像樹的年輪那樣映射到絕對時間軸上。研究團隊證明,GEMINI 在體內可記錄小時級的細胞動態過程,並且連續記錄數天甚至一週以上。
簡單來理解這項技術,它就像在細胞內部安裝了一臺生長記錄儀。只要細胞每次經歷信號變化,都會在該結構上留下新的“時間條紋”,最終成爲可記錄、可回放的細胞“錄像”。
更重要的是,“記憶體”由細胞自己“生產”,並把自己經歷過的事情寫入記憶體的結構中。它最大的優勢在於,每個細胞都能擁有獨有的記憶體,爲全器官的動態解析提供了可能性。
“GEMINI 在腫瘤異種移植模型中能夠實現全腫瘤的表達與記錄,這是以往工具難以實現的能力,我們希望這項技術能爲細胞生物學與神經科學研究打開新的實驗範式,並創造更多的可能性。”林鼎昌對 DeepTech 表示。

圖丨左至右:林鼎昌(通訊),嚴宇清(共同一作),陸家禧(共同一作),李喆(共同一作)(來源:受訪者)
近日,相關論文以《遺傳編碼的組裝式記錄儀實現細胞歷史的時間分辨解析》(Genetically encoded assembly recorder temporally resolves cellular history)爲題發表在 Nature[1]。約翰斯·霍普金斯大學博士生嚴宇清、陸家禧和華盛頓大學李喆博士(現南方科技大學教授)是論文共同第一作者,林鼎昌教授擔任通訊作者。

圖丨相關論文(來源:Nature)
給細胞裝上“記錄儀”,打破生命黑箱
傳統的終點分析方法如同拍攝一張靜態圖片,只能解析某個特定時刻的狀態,卻看不到細胞走到這一步的具體步驟。實際上,很多關鍵過程發生在更早之前,而終點分析往往忽略了這些重要的細節。
相反,實時熒光成像(長時間盯拍)能夠彌補傳統終點分析的短板,可像拍攝視頻那樣提供高清晰的動態過程。但其難點在於必須長期盯着同一批細胞:在真實組織裏,細胞密度往往很高且三維空間排布,由於它們在體內是高度動態的,因此難以精準定位。
此外,活體組織通常是不透明的,熒光成像難以覆蓋深層組織,信號會受散射影響,還存在光毒性和漂白問題,時間越長越難保持信號穩定。最後或許能夠在單細胞層面看得很清楚,但也只限於在很短時間內看到了很少數量。
那麼,在器官尺度的組織微環境中,究竟關心什麼時間尺度的動態過程?在某些組織以及特定的科學問題中,超快的信號(例如腦部神經電生理)很有必要,但在更多的情況下,分鐘到小時尺度的時間分辨率對於細胞動態追蹤和分析已經足夠。
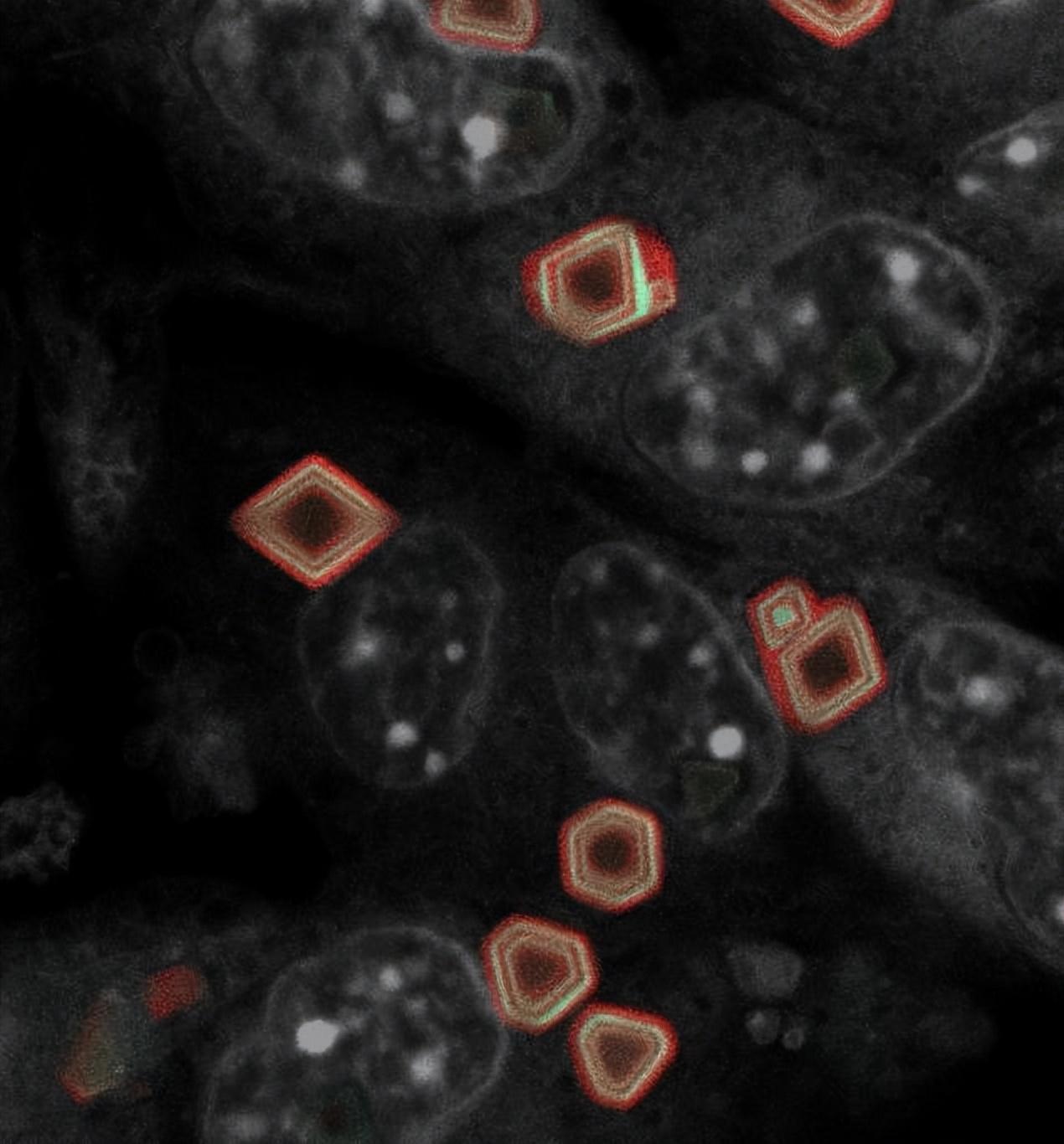
(來源:Lin Lab)
研究團隊提出,在這種時間尺度下,“實時盯梢”或許並不是最優解,特別是當關心細胞的空間分佈以及希望對組織中大量甚至所有細胞同時監測的情況。於是,他們將研究重點放在“事後回溯”上。
林鼎昌解釋道:“GEMINI 的本質是一個終點分析方法,我們的想法是,如果我們能夠把時間信息帶回到固定的組織樣品中,則完全有可能在高通量、空間信息保留的情況下,實現在小時甚至分鐘時間尺度下的單細胞動態解析。”
把“年輪”裝進細胞,空間和時間終於能兼得
多年來,科學家嘗試開發了各種基於基因編輯的核酸類記錄工具。這些工具雖然在細胞譜系示蹤方面具有重要應用,但它在細胞活動的實時追蹤方面有幾個致命短板:基因編輯的動力學較慢,導致難以捕捉小時級或更快的動態過程;目前編輯的效率不高,導致有些細胞標記不完全,缺乏單細胞分辨率;基於測序的讀取通常需要破壞組織結構,導致空間信息的丟失。
GEMINI 作爲一個基於蛋白的記錄工具,把“寫入”變成一個更直接的過程:細胞把信號轉成某種帶熒光的蛋白表達,這些蛋白會被“實時”收進生長結構裏。讀出則是直接在原位看到紋理,從而把空間與時間儘可能同時保留下來。
之前,林鼎昌團隊曾經開發了基於線性蛋白組裝的胞內記錄工具 [2]。然而,對於線性蛋白組裝來說,它的讀取精度很大程度取決於空間取向,當線性蛋白不在焦平面上,難以通過二維成像可靠地讀取信息。GEMINI 的其中一項創新在於採用三維各向同性生長方式,信息在各個方向的記錄是一致的。因此,無論它空間取向如何均能可靠讀出信息,爲高通量讀取與分析提供了可行路徑。
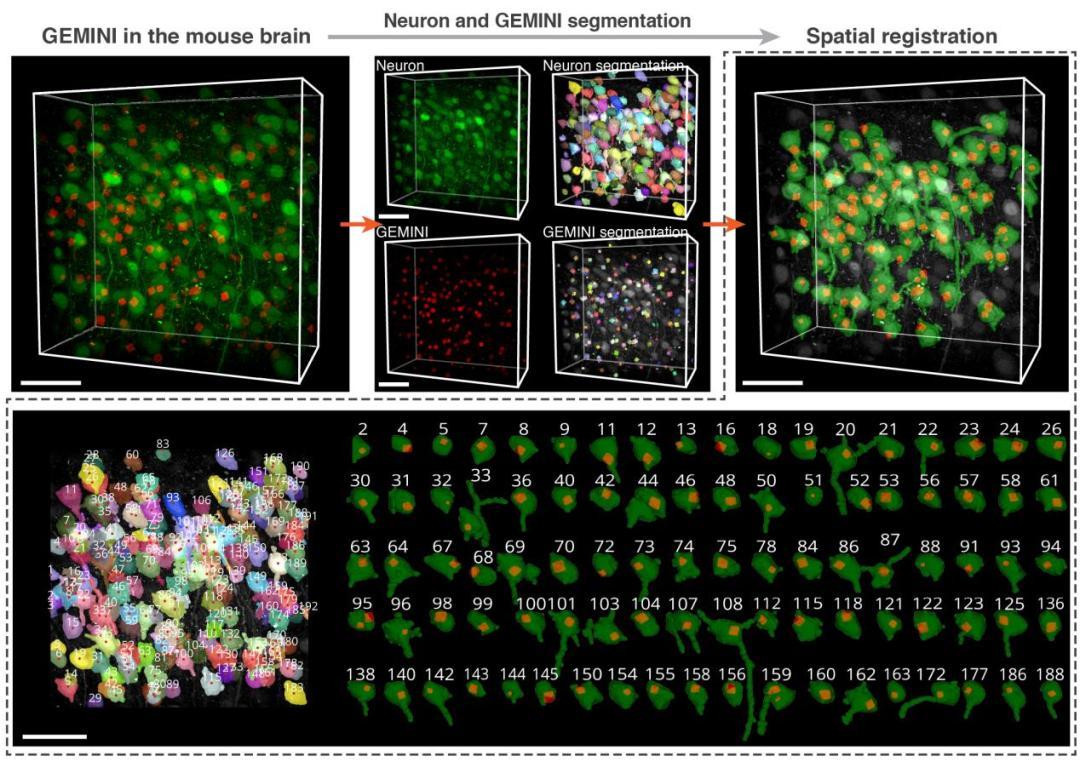
(來源:Nature)
從 GEMINI 記錄的原理來看,它與樹木用年輪記錄具有異曲同工之妙。二者的共同點在於在生長過程中把信息記錄下來:年輪每過一年增加一圈,而 GEMINI 每經歷一段細胞時間就會增加一圈熒光條紋。不同之處在於,年輪圈數用於判斷地理事件發生的時間,而 GEMINI 記錄的是細胞的動態歷史,通過對應的“時間戳”幫助回溯事件發生的時間。
最難的不是設計,是讓蛋白質“剛剛好”開始生長
據研究團隊介紹,這項研究中最大挑戰在於如何調控蛋白質自組裝的形核過程。他們不希望形核太容易,因爲形核太容易常常會在同一個細胞內形成多個核互相競爭生長,給後續解析帶來難題。與此同時,也不希望形核太難,否則形核時間點會非常滯後且不同步,影響時間窗口的確定。現實中這個形核能的窗口很小,需要通過精細的蛋白設計結合蛋白工程/篩選來尋找。
此外,通過形核能的篩選的蛋白質並不一定適合作爲 GEMINI,它還需要蛋白自組裝對細胞的擾動儘可能小。研究團隊在篩選方面投入了大量的精力,最後得到了論文中使用的版本,這是在結合了形核能優化及細胞兼容性篩選之後最優的版本。
回憶 GEMINI 從無到有、從概念到實物的過程,林鼎昌說道:“現在回想起第一次在細胞內得到漂亮的蛋白自組裝以及第一次在小鼠大腦中表達成功的時刻,仍然讓我們感覺興奮不已,並第一時間與遠在西雅圖的合作者們分享了這個結果。”
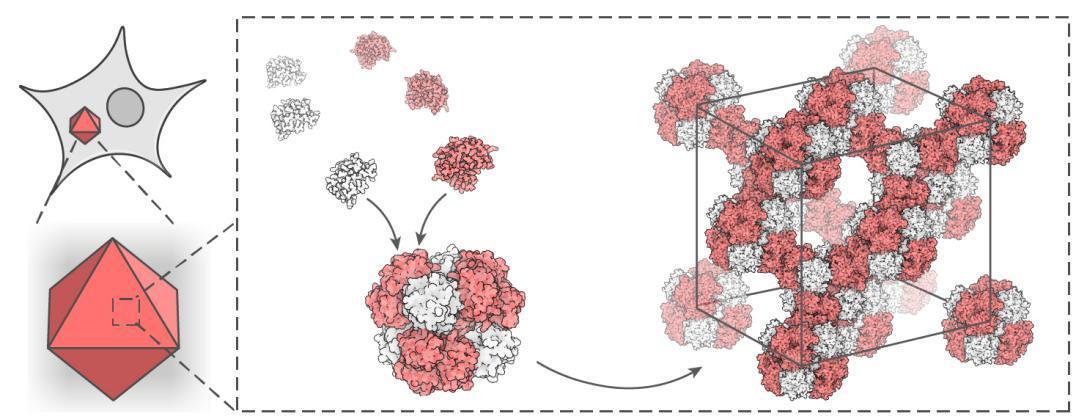
(來源:Nature)
但研究團隊並沒有駐足於此,直到他們第一次用自主構建的簡單模型近乎完美地解析了時間的信息。
“這是一個相當意外的結果。我們當時並沒有想到能這麼準確,畢竟相比於一維生長,三維生長的過程是非線性的,這給解析帶來了一定的難度。”林鼎昌表示。
實際上,研究團隊很早就做好了心理建設,準備好幾套方案來解決這個難題(例如用機器學習方法)。他坦言,能夠用一個簡單的模型進行解析,讓我們重新認識了胞內自組裝的過程,以及它的可靠性和可重複性。
大腦活動、腫瘤演化,終於有了“回放鍵”
值得關注的是,在培養細胞中,GEMINI 能分辨間隔 15 分鐘的信號,對炎症因子的檢測靈敏度比傳統方法高出 2 個數量級。在體內驗證中,GEMINI 在細胞、組織以及動物行爲層面均表現出優異的組織相容性。
研究人員進一步將其用於記錄,並回溯腫瘤異種移植(xenograft)中炎症相關通路的時空響應圖譜,在小鼠大腦中實現了對轉錄及癲癇相關信號的時空信息記錄。
15 分鐘分辨率意味着,很多過去會被看成“一次持續激活”的過程,現在可以拆成更細的脈衝、間歇與先後次序。對於許多信號通路來說,細胞並不是只在乎有沒有信號,而是更在乎信號是瞬時的、反覆的,還是持續的。“分辨率顯著提升後,我們更容易將不同的動態模式和不同的細胞命運建立對應關係。”林鼎昌說。
靈敏度提高意味着以前必須用很強的刺激、才能在羣體平均裏看到變化;現在可以在更接近真實生理水平的條件下,捕捉微弱但關鍵的事件。
一個直觀例子是,在癌細胞耐藥中,一些耐藥並不是突然獲得,而是經歷了多輪壓力後逐步進入一種保護狀態。林鼎昌進一步指出,過去我們常看到的是最後活下來的細胞是什麼樣,但不知道它們此前經歷了多少次、什麼節奏的應激。現在我們有機會在同一個腫瘤微環境裏,把不同細胞經歷過的刺激歷史拉出來對比:耐藥細胞是否更像多次短暫刺激的累積結果,還是來自某一次強刺激觸發。
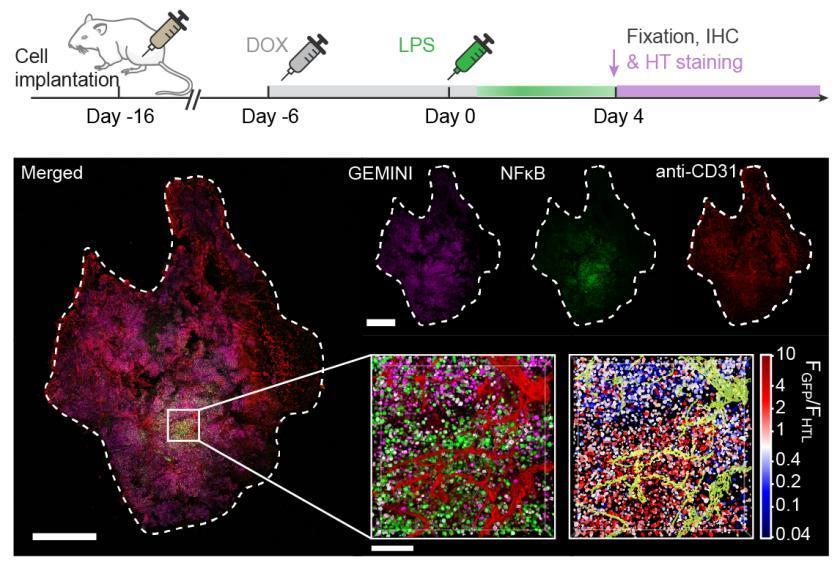
(來源:Nature)
生命體系的很多關鍵問題都是受制於時間分辨率。“目前,我們已經能非常精準測到基因表達、蛋白丰度、空間位置,但在很多真實場景裏,細胞最在乎的恰恰是動態過程:刺激出現的節奏、持續時間、間隔、疊加順序。”林鼎昌說。
空間和時間信息的結合可能會帶來顛覆性的認知,GEMINI 的定製化細胞內器件有望應用於腫瘤與免疫、大腦研究和胚胎髮育與再生等領域。
同一腫瘤裏細胞處在不同的氧氣、營養、免疫壓力下,信號高度不均一。將動態記錄擴展到整個組織尺度,有可能爲回答什麼樣的刺激歷史更容易導向侵襲、轉移或免疫逃逸提供支持。
神經系統裏很多過程並非一次事件,而是長期活動模式的累積。如果能在空間上覆蓋更大區域、在時間上保留活動歷史,就可能把“哪類活動模式”與“哪類可塑性或行爲改變”更直接地對應起來。
發育過程中的先後順序尤其重要。空間上相鄰的細胞,因爲經歷的信號節奏不同,可能走向完全不同的分化路線。如果能把歷史寫下來,有望幫助研究人員將發育的因果鏈拉直。
不只是記錄,GEMINI 正在變成一個可編程平臺
研究團隊認爲,從原理上來看,只要某種細胞狀態或事件能夠通過啓動子/轉錄調控轉換成報告亞基的表達變化,就有機會被 GEMINI 寫入。因此它更像一個可編程的平臺:可通過更換“觸發開關”記錄不同通路、不同應答、不同細胞類型特異的事件。
在下一代 GEMINI 開發中,研究團隊希望實現更長時間窗口、更穩定的寫入,讓記錄能可靠拓展到更長時間,同時降低背景與細胞負擔。與此同時,他們還致力於向更高的可編程性與通用性方面發展,即把“換一個啓動子就能記錄另一類事件”做得更標準化、更易用,並降低不同實驗室遷移的門檻。
“我們希望未來能夠在更復雜的組織與疾病模型中檢驗它的價值,包括更大尺度的空間覆蓋、更真實的微環境干擾下是否仍能清晰讀出時間線。最終,讓更多人使用 GEMINI,儘可能讓該工具幫助拓寬知識的邊界。”
參考資料:
1.https://www.nature.com/articles/s41586-026-10323-y
2.https://www.nature.com/articles/s41587-022-01524-7
運營/排版:何晨龍





